-
Химики раскрыли секрет натриевых взрывов
25.12.2015
 Hi-tech
Hi-tech -
Одним из самых зрелищных опытов в классе химии есть реакция натрия с водой — в то время, когда преподаватель бросает мелкий кусочек металла в воду, происходит взрыв. Учители выполняют данный опыт на глазах ликующих учеников десятилетиями, но, как выяснилось на протяжении нового изучения, сама реакция, стоящая за взрывом, продолжительное время понималась неправильно.
Ведущий создатель нового изучения Павел Юнгвирт (Pavel Jungwirth) вместе с сотрудниками из Чешской академии наук в Праге опубликовал, возможно сообщить, революционную статью в издании Nature Chemistry.
Как поясняют исследователи, взрыв есть не только следствием воспламенения водорода, но и освобождения щелочных металлов от воды. По сути, реакция представляет собой стремительный финал электронов с последующим взрывом металла, обусловленный электрическим отталкиванием.
Натрий — это серебристый металл, что остаётся довольно жёстким при комнатной температуре. Если он приходит в контакт с водой, то на протяжении реакции появляется водород и гидроксид натрия.
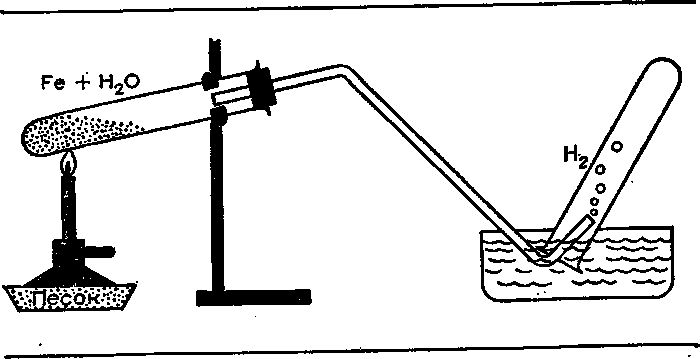 Подобная «взрывная» реакция отмечается и у калия, лишь она оказывается ещё более замечательной.
Подобная «взрывная» реакция отмечается и у калия, лишь она оказывается ещё более замечательной.На протяжении этих реакций выделяется много тепла, исходя из этого продолжительное время химикам казалось, что взрывы результат воспламенения водорода.
«Чтобы получить зрелищный взрыв на протяжении химической реакции, реагенты нужно смешать скоро и действенно. При с щелочными металлами, но, пар и водородный газ, каковые образуются на поверхности металла, должны предотвращать попадания на эту поверхность громадного количества воды. А без постоянного пополнения запасов воды реакция обязана скоро сойти на нет», — поясняет Юнгвирт.
Опыт проводил сотрудник Юнгвирта Филип Мейсон (Philip Mason). Он учёл, что натрий время от времени (к примеру, при неправильном хранении) может окислиться на поверхности и не взорваться, и для получения желаемой реакции, применял в собственном опыте сплав калия и натрия. Сплав является жидкостьюпри комнатной температуре.
Мейсон капнул сплав в стакан с водой и заснял целый процесс на скоростную камеру. После этого учёные, наконец, вычислили, что именно провоцирует бурную реакцию на ранних стадиях.
Реакция начинается меньше чем через миллисекунду по окончании того, как железная капля, выпущенная из шприца, соприкасается с водой. Спустя всего 0,4 миллисекунды металл начинает выстреливать «шипами», и происходит это через чур скоро, дабы быть позванным одним только теплом, делают вывод учёные.
Более того, между 0,3 и 0,5 миллисекундами около железных шипов в жидкости образуются светло синий-фиолетовые тучи. Ранее аналогичного химики не подмечали.
Исследователи совершили квантово-механическое компьютерное моделирование процесса с условием, что в реакции было задействовано всего 19 атомов натрия. Исследователи поняли, что любой из атомов на поверхности металла теряет электрон в течение всего нескольких пикосекунд, и что эти электроны «выстреливают» в окружающую воду, где они окружаются молекулами воды.
Сольватированные электроны, как уже известно, имеют глубочайший светло синий цвет, что непродолжительное время и отмечается на записи.
Финал электронов оставляет кусок металла полным положительно заряженных ионов, каковые отталкивают друг друга. В итоге происходит кулоновский взрыв, при котором металл разлетается на части в силу обоюдного электростатического отталкивания ионов, делают вывод чешские учёные.
Случайные записи:
- Молекулярные очки против слепоты
- Молодому учёному нгту вручили грант юнеско в области «зелёной химии»
What If You Drop Sodium In Gasoline? Will It Explode?
Похожие статьи, которые вам понравятся:
-
Ученые раскрыли мужчинам секреты правильного танца
Мы уже писали ранее об опыте, что совершила несколько европейских исследователей, продемонстрировавшем, что дамы, выбирая мужчин, предпочтут хорошего…
-
Бесконечная пустота или большой взрыв: как вселенная закончит свое существование?
Кроме того, что ученые не уверены в том, как Вселенная закончит собственный существование, они кроме того не уверены, закончит ли она его по большому…
-
Сердечные секреты раскроют издалека
В поход и на дачу возможно без страха отправиться любому, в случае если захватить с собой мобильный кардиограф. В Пущинском Национальном Университете…
-
Коллайдер воссоздал большой взрыв, в результате которого образовалась вселенная
Громадному андронному коллайдеру удалось воссоздать Громадный Взрыв в миниатюре, разбивая атомы свинца на еще более небольшие частички. Полученная в…



