-
Старению добавили новую причину
06.02.2018
 Наука и жизнь
Наука и жизнь -
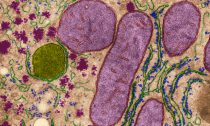
С возрастом белки в клетке начинают не хорошо сворачиваться из-за трансформаций в окислительно-восстановительном потенциале в местах сборки протеиновых молекул.
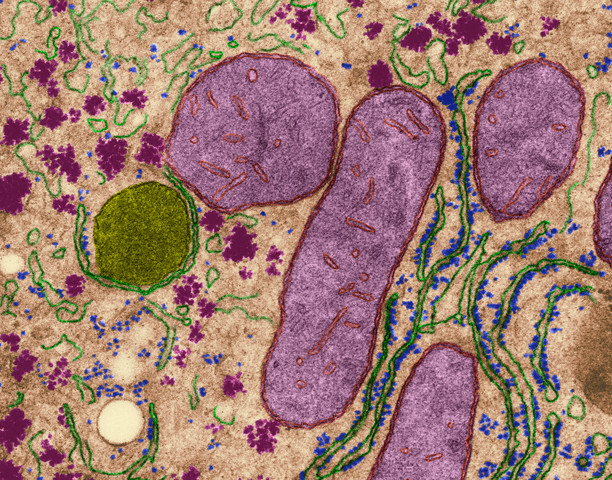
Клетка печени; элементы эндоплазматической сети – зелёные «нити», усаженные светло синий точками – рибосомами, синтезирующими белок. Громадные сиреневые пятна – митохондрии. (Dennis Kunkel Microscopy, Inc. / Visuals Unlimited / Corbis.) Мембранные «стопки» эндоплазматического ретикулума с рибосомами. (Фото Lester V. Bergman / CORBIS.)‹ ›
Старение тела начинается со старения его клеток, а с чего начинается старение клеток? биологи и Медики до сих ещё не знают всех обстоятельств, не смотря на то, что многие читатели точно отыщут в памяти о самых известных теориях старения, в которых говорится про митохондрии и теломеры.
С одной стороны, как мы знаем, что теломерные участки, защищающие финиши хромосом, сокращаются с каждым делением, так что клетка может свободно делиться некое ограниченное число раз, по окончании чего у неё начнут повреждаться ответственные гены, примыкающие к оголённым хромосомным финишам.
 И процессы старения связывают частично с укорочением теломер.
И процессы старения связывают частично с укорочением теломер.Иначе, клеточные митохондрии, не смотря на то, что и снабжают нас энергией, в качестве побочного результата являются неиссякаемым источником агрессивных молекул-окислителей – кислородных радикалов, повреждающих белки, ДНК, другие биомолекулы и липиды мембран. В большинстве случаев клетке имеется что противопоставить окислительному стрессу, но со временем антиоксидантные механизмы слабеют (отдельный вопрос, само собой разумеется, из-за чего они слабеют), и окислительный стресс делается всё посильнее, на уровне организма становясь обстоятельством возрастных болезней.
Но, как мы знаем, в живой материи всё взаимосвязано, и было бы необычно, если бы процессы старения зарождались обособленных участках клетки, не затрагивая другие её отделы. Как продемонстрировали опыты Янины Кирштайн (Janine Kirstein) из Лейбницевского университета молекулярной фармакологии и её сотрудников из Японии и США, одним из самых замечательных «источников старения», в случае если возможно так сообщить, помогает эндоплазматический ретикулум, либо эндоплазматическая сеть (ЭР, либо ЭС). Он (либо она) являются сложную разветвлённую сеть мембранных каналов, цистерн и пузырьков, и в школьных книжках биологии говорится, что на мембранах эндоплазматической сети, обсаженных рибосомами, идёт синтез протеиновых молекул и сворачивание готовых протеиновых молекул в верную пространственную конформацию.
Аминокислоты, входящие в состав протеиновой молекулы, взаимодействуют между собой и с окружающим раствором, кое-какие притягиваются, кое-какие отталкиваются, в следствии полипептидная цепочка получает так именуемую третичную структуру – сворачивается в очень сложно устроенный клубок. Как раз в таком виде белок, будь то фермент, белок-транспортёр и т. д., может делать собственную функцию (к примеру, деятельный центр ферментов, в которых происходит расщепление субстратных молекул либо сшивание их совместно, формируется именно в следствии пространственного сворачивания аминокислотной цепочки).
Одна из самые известных «скрепок», помогающая белку держатся в свёрнутом состоянии – ковалентная связь между атомами серы, входящими в состав аминокислоты цистеина. Образующиеся дисульфидные мостики смогут сближать достаточно удалённые участки полипептидной цепи; и такие связи нужны для функционирования самых различных белков, а также антител и инсулина.
Дисульфидные сшивки образуются в эндоплазматической сети, в которой имеется нужные физико-химические условия. Окислительно-восстановительный потенциал (не путать с кислотностью!) в совокупности мембранных цистерн и каналов сдвинут в окислительную сторону, так что атомы серы из цистеинов легко смогут образовать между собой ковалентную сообщение. Но, как пишут авторы работы в EMBO Journal, со временем окислительно-восстановительный потенциал в эндоплазматической сети теряет окислительные свойства, почему белки перестают сворачиваться и трудиться, как нужно.
Это растолковывает многое: известно, к примеру, что с возрастом появляется всё больше неправильно свёрнутых протеиновых молекул, что многие секреторные белки становятся нестабильны и перестают функционировать при мельчайшем стрессе; кроме того возрастное ослабление иммунитета возможно растолковать смещением окислительно-восстановительного потенциала, потому, что антитела перед выходом из клетки не смогут зафиксировать нужную пространственную структуру. (Одновременно с этим в окружающей цитоплазме всё происходит напротив: окислительный потенциал среды растёт и улучшается пресловутый окислительный стресс, в результате которого портятся белки.)
Непорядки в работе эндоплазматической сети смогут случаться и при стрессе и приводить к тем же последствиям – накоплению неправильно свёрнутых молекул белка. Тут стоит отыскать в памяти, что нейродегенеративные болезни, такие, как синдром Альцгеймера, синдром Паркинсона, синдром Хантингтона, появляются именно по вине белков с неправильной пространственной структурой.
И тут также, по словам исследователей, всё начинается с неприятностей в окислительно-восстановительном потенциале эндоплазматической сети. Более того, как выяснилось, патогенные молекулы белков, показавшись в одних тканях, смогут приводить к в окислительно-восстановительном потенциале вторых тканей, ускоряя тем самым процессы старения.
В молекулярной и клеточной биологии в действительности достаточно давно существует понятие ЭР-стресса (стресса, связанного с эндоплазматическим ретикулумом), в то время, когда в клетке внезапно начинают деятельно накапливаться белки с неправильной укладкой. Новые опыты разрешили связать ЭР- стресс с процессами старения и с физико-химическими неполадками в ответственном клеточном органоиде.
Испытания ставили на червях-нематодах, которых модифицировали так, дабы возможно было смотреть за трансформациями окислительно-восстановительного потенциала в различных участках клеток. Но, учитывая, что синтез его сворачивание и белка происходят у всех организмов, имеется все основания считать, что возрастные трансформации в эндоплазматической сети имеют место и у человека.
Само собой разумеется, всё это лишь усложняет картину старения, но, иначе, в биологии по большому счету почти никогда не бывает «одной основной обстоятельства» чего бы то ни было, постоянно приходится разглядывать целый пучок следствий и причин. И чем больше мы будем тут знать, тем правильнее сможем определять стадию и динамику старения, а в том месте, смотришь, и до вечной юности как-нибудь доберёмся.
По данным Phys.org.
Создатель: Кирилл Стасевич
Источник: nkj.ru
Cartoon — C U Again feat. Mikk Mäe (Cartoon vs Futuristik VIP) [NCS Release]
Похожие статьи, которые вам понравятся:
-
Сила новой мысли от hyundai: концепт-гибрид i-oniq покоряет женеву
Технологические инновации в сфере транспортных средств сейчас перешагнули по значимости кроме того классические средства сокращения потребления горючего,…
-
Угроза: мыстановимся устойчивы кантибиотикам
Доклад председателя совета директоров ВОЗ Маргарет Чен «Устойчивость к противомикробным препаратам в ЕС и в мире» на прошедшей в 2012 году в Копенгагене…
-
Квантово-механические расчеты оказывают помощь целенаправленно изменять свойства полициклических ароматических соединений. Полициклические ароматические…
-


