-
Новая жизнь старых клеток дает надежду
19.07.2011
 Наука и жизнь
Наука и жизнь -
Индуцированные плюрипотентные стволовые клетки – надежда человечества если не на вечную юность, то, по крайней мере, на решение многих медицинских неприятностей. О том, какие конкретно практические возможности существуют у его открытия, поведал нобелевский лауреат доктор наук Синья Яманака.
В 2012 году Синья Яманака вместе с Джоном Гардоном взяли Нобелевскую премию за открытие того, что зрелые клетки возможно «перепрограммировать» обратно в стволовое плюрипотентное состояние . Сам способ обращения зрелых клеток в стволовые показался за шесть лет до премии, в 2006 году, по окончании чего все сходу заговорили о широчайших возможностях, раскрывающихся перед биологией и медициной. О будущем способа и о тех изучениях, каковые проводятся в руководимом им Центре применения и изучения индуцированных плюрипотентных клеток (Center for iPS Cell Research and Application) в Японии, доктор наук Яманака поведал на открытой лекции, прошедшей 29 мая в стенках Петербургского Политехнического университета.
Доктор наук Синья Яманака на протяжении лекции (фото Юлии Смирновой).
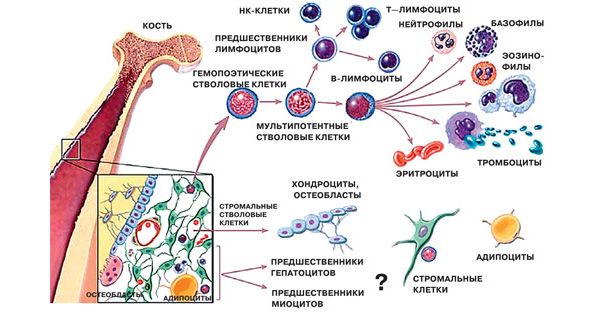
В юности будущий нобелевский лауреат желал стать доктором. Он взял медицинское образование и докторскую степень по медицине, а также работал врачом-ортопедом. Но позднее Синья Яманака сделал вывод, что принесёт больше пользы, в случае если начнет заниматься наукой. Во второй половине 90-ых годов двадцатого века Джеймс его сотрудники и Томсон из Висконсинского университета в Мадисоне в первый раз взяли линию людских эмбриональных стволовых клеток (ЭСК).
Потенциал стволовых клеток для применения в медицине ученые оценили сходу: если бы удалось заменить пораженные ткани и клетки новыми, выращенными из стволовых клеток, то возможно было бы решить проблему с целым рядом серьёзных болезней. Но существовала этическая неприятность – так как ЭСК возможно добыть лишь из людских эмбрионов.
Спустя год в технологии и Институте науки Нара (Япония) стволовыми клетками начал заниматься Яманака. Он решил ответить на вопрос: в случае если из стволовой клетки возможно взять фактически любую клетку организма, то запрещено ли вынудить зрелую, специальную клетку превратиться во что-то второе? Ученый думал, что поиск механизма, что сможет вынудить клетку переродиться, займет всю его оставшуюся судьбу.
Но уже через 6 лет он и его сотрудники взяли результаты, каковые скоро удостоились Нобелевской премии.
Способ получения индуцированных плюрипотентных стволовых клеток (ИПСК) с 2006 года был усовершенствован, и сейчас перепрограммированию возможно подвергнуть, к примеру, кое-какие клетки крови, забранные из несложного клинического примера. Переходя от теории к практическому применению разработки, доктор наук показал необычные кадры: на экране показалась пульсирующая ткань. Это, как пояснил Яманака, ткань сердечной мускулы, которую вырастили в лаборатории из одной клетки крови, обращённой в стволовое состояние.
На сегодня существует три главных направления применения ИПСК. Первое – in vivo, в клеточной терапии, в то время, когда ветхие больные клетки пробуют заменить на новые, дифференцированные и здоровые. Второе – in vitro, в то время, когда из ИПСК приобретают различные виды специальных клеток для тестирования разных фармакологических препаратов, лекарств, токсинов и т.д.
Третье направление – создание банка людских тканей с разными генетическими недостатками для нахождения и изучения дорог вероятного лечения генетических заболеваний.
Как мы знаем, что кое-какие болеутоляющие и антибиотики в качестве побочного результата приводят к аритмии, которая в тяжёлых случаях ведет к летальному финалу. Посредством ИПСК возможно более шепетильно тестировать антиаритмические препараты, поскольку дабы проверить безопасность и токсичность препарата на сердечной мышце, не требуется добывать клетки прямо из людской сердца, их возможно в лаборатории.
на данный момент для таких тестов употребляются среди них и раковые клетки, в которых активирован ген, кодирующий клеточный калиевый насос – данный насос нужен для работы сердечной мускулы. Так возможно изучить внутреннюю физиологию и калиевую проницаемость клетки в ответ на воздействие того либо иного компонента лекарственного препарата.
Еще один показательный пример – боковой амиотрофический склероз (БАС), при котором происходит прогрессирующее поражение моторных нейронов, сопровождаемое атрофией мышц и параличом конечностей. Один из самых известных больных БАС – ученый-космолог Стивен Хокинг.
В возглавляемом доктором наук Яманака университете удалось взять ИПСК больных и здоровых людей БАС. В самих стволовых клетках никаких различий не нашли. Но по окончании того, как эти клетки превратились в моторные нейроны, отличия нашлись. Оказалось, что отростки нейронов у больных БАС были вдвое меньше, чем у здоровых людей.Сейчас на выращенных в лаборатории больных нейронах тестируют вещества, каковые, быть может, смогут обратить вспять процесс укорочения нейронных отростков.
Третий путь применения ИПСК – то самое, что когда-то побудило ученого заняться стволовыми клетками, клеточная терапия. Ученые видят громадные возможности в применении ИПСК для посттравматического восстановления спинного мозга, в то время, когда поврежденные клетки заменяются на новые здоровые. Успешные испытания на мышах разрешают сохранять надежду, что через пара лет данный способ возможно будет опробовать и на человеке.
Уже в конце 2014 года начнутся клинические изучения по применению ИПСК в лечении дегенерации сетчатки, одной из обстоятельств старческой слепоты. Потому, что за глазом весьма комфортно замечать, на протяжении этого изучения ученые сохраняют надежду решить еще один вопрос. Имеется важные опасения, что ИПСК не в полной мере надёжны, поскольку смогут пойти по неверному пути, преобразовываясь вместо обычных специальных клеток в раковые.
За клетками сетчатки весьма комфортно замечать, и, в случае если хотя бы одна клетка постарается организовать злокачественную опухоль, это возможно будет сразу же подметить и удалить «отщепенца» посредством лазера. Но, доктор наук Яманака уверен в том, что не смотря на то, что опасения относительно рака оправданы, риск таких отклонений минимален, и пользы от применения ИПСК в клинической практике будет неоспоримо больше, чем потенциального вреда.
Еще одна неприятность, которую возможно решить посредством ИПСК – дефицит донорской крови. Доктор наук приводит в пример Японию, где сейчас отмечается заметное старение нации и людям все чаще и чаще требуется переливание крови. Новые разработки смогут обеспечить клиники не просто достаточным числом крови, но и отдельными типами клеток.
Возвращаясь к замене больных клеток здоровыми, направляться упомянуть про ещё одно преимущество ИПСК. Простая головная боль трансплантологов – это отторжение пересаженных тканей, но с ИПСК об этом возможно не тревожиться – так как исходный материал заберут от самого больного, и клетки, полученные из ИПСК, будут для его иммунитета «собственными». Но такие технологии до тех пор пока еще не через чур дёшевы и требуют большое количество времени для исполнения, а ведь при острых состояний время от времени счет идет на часы и дни.Но оказалось, что эту проблему возможно решить, в случае если применять для получения ИПСК не только собственные клетки, но и донорские, подходящие по главному комплексу гистосовместимости (HLA, от британского «Human Leucocyte Antigens» – человеческие лейкоцитарные антигены).
Антигены HLA играются наиболее значимую роль в регуляции иммунного ответа на чужеродные антигены и сами являются сильными антигенами. По ним иммунитет определяет «собственных» и «чужих», и несовпадение реципиента и донора по HLA ведет к отторжению пересаженных органов. Всего существует более 100 типов таких антигенов.
Оказалось, что при с ИПСК донором возможно человек гомозиготный по определенному типу HLA, а реципиентом – гетерозиготный, другими словами не обязательно искать полностью полного иммунного совпадения. Отыскать достаточное количество потенциальных доноров кроме того в не большой Японии – огромное дело. По словам доктора наук, это должна быть масштабная акция, в которой примет участие большинство обитателей страны.
Но в случае если удастся отыскать всего лишь 140 гомозиготных доноров, этого хватит, дабы обеспечить ИПСК 90 процентов населения.
Создатель: Юлия Смирнова
Источник: www.nkj.ru
Случайные записи:
Новая жизнь старых вещей. 5 советов от мастеров «Фазенды»
Похожие статьи, которые вам понравятся:
-
Молодое окружение возвращает к жизни старые стволовые клетки
Взрослые стволовые клетки смогут взять новую судьбу, в случае если их выращивать в окружении молодых клеток, по крайней мере, у мышей. Данное открытие…
-
Фабрика жизни: стволовые клетки
Секрет судьбы Один из авторов еще одного наиболее значимого открытия XX века — биофизик и американский генетик Джеймс Уотсон — позирует на фоне модели…
-
Удаление старых клеток может продлить жизнь человека
Новое изучение, совершённое на мышах, показывает, что удаляя изношенные клетки организма (стареющие клетки) пара раз за судьбу мышей, исследователи…
-
Новый способ получения стволовых клеток из жировой ткани
Исследователи из Медицинской школы Стэнфордского университета (США) создали достаточно действенную разработку преобразования клеток, в которой для…
-



