-
Генетическое редактирование предотвращает слепоту
13.05.2016
 Наука и жизнь
Наука и жизнь -
Посредством способа генетической модификации CRISPR удалось затормозить смерть фоторецепторов в сетчатке у мышей.
Способ редактирования генома называющиеся CRISPR (либо CRISPR/Cas) в последние два года стал одной из самых обсуждаемых тем в науке. Его в прямом смысле позаимствовали у бактерий: в собственном природном виде механизм CRISPR/Cas помогает для разрушения вирусной ДНК в бактериальной клетке.
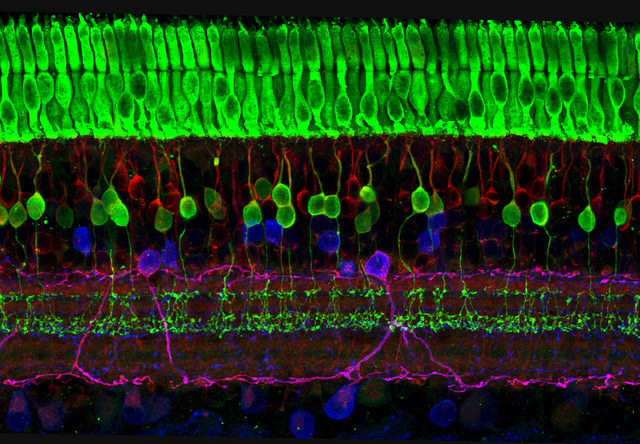
Сетчатка глаза организована несколькими десятками типов клеток, каковые уложены в ней в пара слоев, зеленый клеточный слой – колбочки и фоторецепторы палочки. (Фото ZEISS Microscopy / Flickr.com.)
Дабы отличить вирусную последовательность от собственной, бактерии пользуются достаточно хитроумной молекулярной уловкой, которую молекулярные биологи именно решили применять в собственных целях. Сущность молекулярно-генетического способа CRISPR в том, что, применяя ферменты бактериальной антивирусной защиты, в геном самых различных клеток возможно вносить весьма правильные трансформации.
Как выяснилось, это возможно сделать кроме того для людской эмбриона (по поводу чего целый прошедший год в научном мире бушевали бурные этические дискуссии). Этика этикой, но не следует сбрасывать со квитанций, что с медицинской точки зрения CRISPR-редактирование выглядит весьма и весьма перспективным, поскольку с его помощью возможно исправлять мутировавшие гены, предотвращая тем самым развитие страшных заболеваний.
Как это трудится, возможно проиллюстрировать на примере опытов Ананда Сварупа (Anand Swaroop) и его сотрудников из Национального университета глаза. Исследователи сумели остановить дегенерацию сетчатки у мышей, вынудив посредством CRISPR замолчать один из генов, регулирующих развитие колбочек – и фоторецепторов палочек.
Как мы знаем, палочки и колбочки преобразуют свет в нейронные импульсы: колбочки несут ответственность за цветное зрение и трудятся на ярком свету; палочки, наоборот, оказывают помощь нам видеть, в то время, когда света мало, помимо этого, они питают и поддерживают колбочки. От мутаций чаще страдают палочки, но из-за гибнущих палочек начинают погибать и колбочки. В следствии начинается пигментный ретинит – наследственное дегенеративное заболевание, заканчивающееся полной слепотой.
Ответ как словно бы напрашивается само собой: в случае если у нас имеется способ, разрешающий редактировать гены, то из-за чего бы не исправить мутации в палочках? Так пробовали делать, но кроме того у одного и того же индивидуума вредные мутации в палочках выясняются достаточно разнообразными, а исправить их сходу все практически нереально. Но имеется обходной путь: в статье в Nature Communications говорится, что плохое влияние разнообразных генетических недостатков возможно преодолеть, в случае если отключить у палочек всего один ген – Nrl.
Данный ген кодирует один из множества транскрипционных факторов – так именуются белки, каковые связываются с теми либо иными последовательностями ДНК и так воздействуют на активность генов.
И колбочки, и палочки на протяжении развития сетчатки получаются от одних и тех же клеток-предшественников, и от гена Nrl зависит, кто будет палочкой, а кто – колбочкой. Кроме того, зрелым палочкам ген Nrl нужен чтобы сохранять собственную «палочковость». В случае если ген Nrl замолкает, палочка начинает быть похожим колбочку – но притом, как было сообщено выше, негативные мутации в палочках теряют силу, и в итоге и палочки (не смотря на то, что и похожие на колбочки), и сами колбочки остаются на месте и работают .
Авторы работы применяли редактирование генома по способу CRISPR именно чтобы отключить в палочках ген Nrl. Опыты ставили с мышами, генетически предрасположенными к дегенеративным расстройствам сетчатки. Молекулярные автомобили совокупности генетического редактирования животным вводили посредством особого вируса-носильщика (простой в таких случаях прием) – вирус провозил редактирующие молекулы прямо в клетки сетчатки.
Все случилось так, как и ожидалось: палочки с отключенным Nrl стали похожи на колбочки, наряду с этим сами они прекратили ощущать свет, но оставались в живых и поддерживалии питать колбочки. У пожилых мышей эффект был не сильный, но так или иначе, у всех подопытных животных дегенерация сетчатки, если не остановилась, то хотя бы заметно замедлилась. До тех пор пока что неизвестно, имеется ли тут какие-то отрицательные побочные эффекты, но в случае если их не отыщут в опытах на животных, нет ничего, что помещает начать клинические изучения с больными, страдающими от прогрессирующей слепоты.
Создатель: Кирилл Стасевич
Источник: жизнь и Наука (nkj.ru)
Случайные записи:
Как генетическое редактирование вылечило девочку от рака
Похожие статьи, которые вам понравятся:
-
Редактирование генома применили для лечения слепоты
Ученым удалось исправить генетическую мутацию, которая приводит к дегенеративному заболеванию глаз и слепоту, посредством совокупности редактирования…
-
Тяжелое наследственное заболевание кожи вылечили редактированием генома
Китайские биотехнологи испытали на мышиной модели разработку редактирования генома CRISPR/Cas9 для лечения серьёзного наследственного заболевания кожи….
-
Редактирование генома оружие массового уничтожения
Параграф, касающийся редактирования генома, звучит так: «Исследования редактирования генома, проводимое государствами с иными нормативно-правовыми и…
-
Бактерии и вирусы меняют свой генетический код
Анализ кодонового фагов и словаря бактерий продемонстрировал, что они отходят от канонических значений генетического кода намного чаще, чем считалось….
-


